Perbezaan antara tenaga bon dan entalpi tenaga pemisahan bon
- 3949
- 87
- David Collier
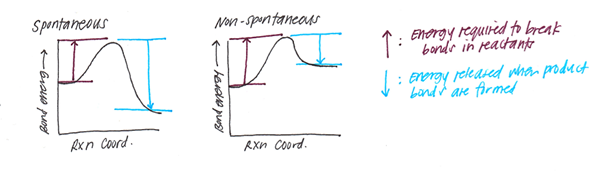
Tenaga bon vs. Tenaga pemisahan bon (entalpi)
Tenaga bon adalah nilai purata tenaga pemisahan bon gas fasa (biasanya pada suhu 298 K) yang ada di antara jenis atom yang sama. Walau bagaimanapun, tenaga pemisahan tenaga dan ikatan bon tidak sama. Tenaga pemisahan bon adalah perubahan entalpi standard apabila ikatan kovalen (juga disebut sebagai ikatan molekul, adalah ikatan kimia antara dua atom bukan logam, yang melibatkan perkongsian pasangan elektron antara atom-atom tersebut) dipotong oleh homolisis (pecahan hingga sama kepingan) untuk memberikan serpihan; yang biasanya spesies radikal. Oleh itu, perbezaan utama antara tenaga bon dan tenaga pemisahan bon ialah tenaga bon adalah nilai purata manakala tenaga pemisahan bon adalah nilai tertentu untuk bon tertentu.
Berapakah tenaga dan tenaga pemisahan bon (entalpi)?
Tenaga bon
Tenaga bon merujuk kepada tenaga yang diperlukan untuk memecahkan semua ikatan yang wujud antara 2 jenis spesies kimia yang sama di sebatian.
Plot tenaga berpotensi sistem 2-atom dan jarak antara spesies kimia menunjukkan jarak di mana tenaga terlalu kurang. Jarak ini diturunkan adalah panjang ikatan antara atom.
Semakin tinggi tenaga bon (e) yang dikaitkan dengan pasangan spesies kimia tertentu, semakin kuat ikatan dikatakan, dan lebih rendah jarak antara 2 atom.
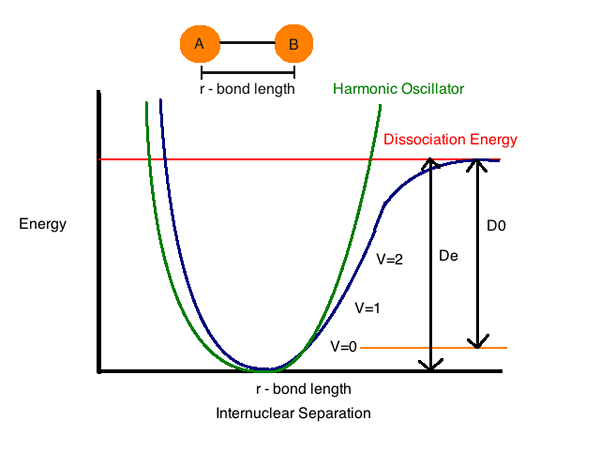
Tenaga pemisahan bon
Tenaga pemisahan bon (entalpi) (h) adalah jumlah tenaga yang diperlukan untuk memecahkan ikatan tertentu dalam homolisis. Kita boleh menentukannya sebagai perubahan entalpi yang berlaku apabila ikatan mengalami belahan oleh homolisis. Tenaga pemisahan bon khusus untuk satu ikatan.
Entalpi bon, (sifat termodinamik sistem) atau tenaga pemisahan bon, disebut sebagai perubahan enthalpy standard apabila ikatan dibersihkan (dipisahkan atau dibahagikan) oleh homolisis (memecahkan kepingan kecil) dengan reaktan dan produk reaksi homolisis pada 0 k (sifar mutlak).
Perbezaan antara tenaga pemisahan tenaga & ikatan bon (entalpi)
Penerangan
Tenaga bon
Tenaga bon juga disebut sebagai entalpi ikatan dan ditakrifkan sebagai ukuran kekuatan ikatan dalam ikatan kimia. Tenaga bon adalah nilai purata
Tenaga pemisahan bon
Tenaga pemisahan bon ditakrifkan sebagai perubahan entalpi standard yang diperlukan untuk memecahkan ikatan kimia
Produk
Tenaga bon
Tenaga bon menawarkan tenaga yang diperlukan untuk membentuk atom yang merupakan bahan permulaan untuk pembentukan bon.
Tenaga pemisahan bon
Tenaga pemisahan bon dengan syarat tenaga yang diperlukan untuk membentuk radikal bebas dari atom yang mencipta ikatan tertentu.
Contoh
Tenaga bon
Dalam kimia, tenaga ikatan (e) atau entalpi ikatan (H) adalah ukuran kekuatan ikatan dalam ikatan kimia.... Sebagai contoh, tenaga ikatan karbon-hidrogen (c-h) dalam metana (CH4) adalah perubahan entalpi yang terlibat dengan memecahkan satu molekul CH4 ke dalam atom karbon (c) dan empat hidrogen (h) radikal, dibahagikan dengan empat.
Tenaga pemisahan bon
Sebagai contoh, dalam molekul metana, tenaga pemisahan bon untuk bon C-H ialah 439 kJ/mol, 460 kJ/mol, 423 kJ/mol dan 339 kJ/mol. Walau bagaimanapun, tenaga bon c-h metana adalah 414 kJ/mol, yang merupakan purata dari semua empat nilai. Selanjutnya, untuk molekul, tenaga pemisahan bon mungkin tidak semestinya sama dengan tenaga bon (seperti contoh metana yang diberikan di atas). Untuk molekul diatom, tenaga bon dan tenaga pemisahan bon adalah sama.
Simbol
Tenaga bon
Ia dilambangkan oleh e
Tenaga pemisahan bon
Ia dilambangkan oleh h
Pembentukan bon
Tenaga bon
Ia memberikan tenaga yang diperlukan untuk membentuk atom yang merupakan bahan permulaan untuk pembentukan ikatan
Tenaga pemisahan bon
Ia memberikan tenaga yang diperlukan untuk menghasilkan radikal bebas dari atom yang menghasilkan ikatan tertentu
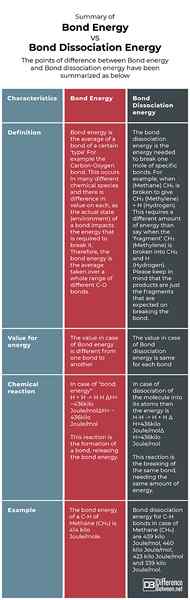
Ringkasan Tenaga Bon vs. Tenaga pemisahan bon
Titik perbezaan antara tenaga bon dan tenaga pemisahan bon telah diringkaskan seperti di bawah:
- « Perbezaan antara bidang kuasa subjek dan bidang kuasa peribadi
- Perbezaan antara perubahan iklim dan pengurangan ozon »

