Perbezaan antara cis dan trans

- 1280
- 8
- Ricardo Koelpin IV
Isomerisme cis-trans terdiri daripada kemungkinan meletakkan kumpulan substituen pada satu atau di sisi yang berlainan satah ikatan berganda atau kitaran bukan aromatik. Isomer cis-trans milik diastereomers kerana mereka bukan cermin refleksi antara satu sama lain. Isomer cis dan trans ditemui di kalangan sebatian organik dan bukan organik.
Nomenclature Cis-Trans menerangkan kedudukan relatif pengganti, dan tidak memberikan penerangan stereokimia, seperti E, z-nomenclature, hanya berkenaan untuk Alkenes.
Kewujudan isomer cis dan trans yang berasingan hanya mungkin disebabkan oleh penghalang tenaga tinggi putaran di sekitar ikatan berganda.

Apa itu cis?
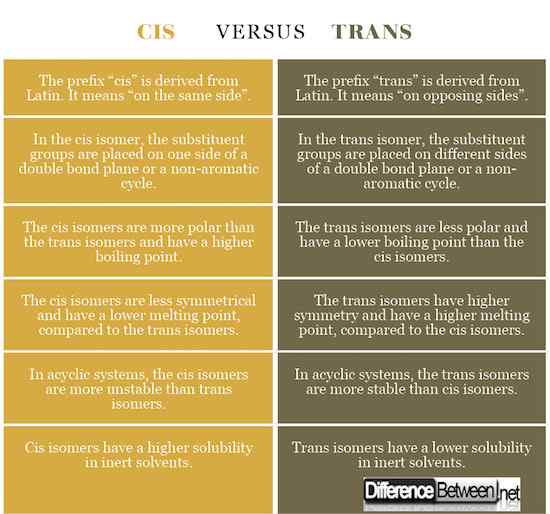
Awalan "cis" berasal dari bahasa Latin. Itu bermaksud "di sisi yang sama". Di dalam isomer cis, kumpulan substituen diletakkan di satu sisi satah ikatan berganda atau kitaran bukan aromatik.
Isomer cis dan trans berbeza dalam sifat fizikal mereka, kerana ketidaksamaan dalam momen dipole keseluruhan dan bentuk molekul.
Titik mendidih relatif ditentukan oleh polaritas. Ia menyebabkan peningkatan daya intermolecular, yang mengakibatkan peningkatan titik mendidih. Isomer cis, yang lebih kutub daripada isomer trans, mempunyai titik mendidih yang lebih tinggi. Perbezaannya boleh menjadi kecil, seperti contohnya dalam alkena dengan rantai lurus. Perbezaan yang lebih besar diperhatikan dalam bahan dengan ikatan kutub. Contoh untuk bahan tersebut ialah 1,2-dichloroethene. Titik mendidih isomer cisnya ialah 60.3 ° C, dan isomer transnya - dengan 12.8 ° C lebih rendah. Sebab perbezaannya ialah dalam isomer cis dua momen c-cl kutub 'momen dipole dan menghasilkan molekul keseluruhan molekul. Akibatnya berlaku daya dipole-dipole intermolecular, yang meningkatkan titik mendidih.
Simetri membolehkan pembungkusan bahan pepejal yang lebih baik. Hasil daripada simetri yang berbeza dari molekul, isomer cis dan trans berbeza dalam titik lebur mereka. Isomer cis, yang kurang simetri, mempunyai titik lebur yang lebih rendah, berbanding dengan isomer trans.
Satu lagi ciri isomer cis ialah mereka mempunyai kepadatan yang lebih tinggi daripada rakan -rakan trans mereka.
Biasanya, dalam sistem aciklik, isomer cis lebih tidak stabil daripada isomer trans. Sebab ini adalah peningkatan dalam interaksi sterik yang tidak menguntungkan dari substituen di isomer cis. Secara umum, isomer cis mempunyai kelarutan yang lebih tinggi dalam pelarut lengai.
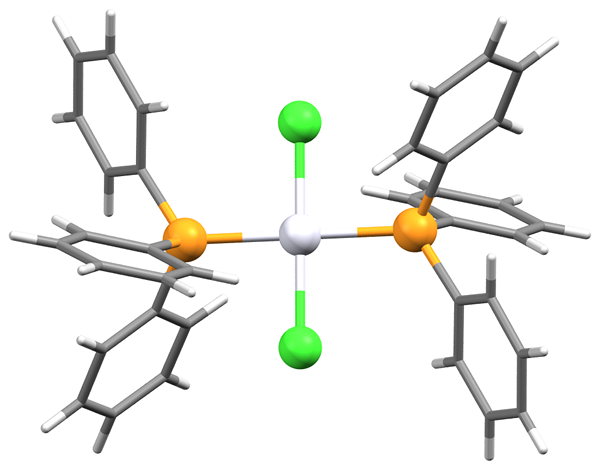
Apa itu trans?
Awalan "trans" berasal dari bahasa Latin. Itu bermaksud "pada pihak lawan". Di dalam isomer trans, kumpulan substituen diletakkan di sisi yang berlainan dari satah ikatan berganda atau kitaran bukan aromatik.
Titik mendidih isomer trans lebih rendah daripada isomer cis. Perbezaannya lebih penting dalam bahan dengan ikatan kutub. Di dalam isomer trans 1,2-dikloroethene, kedua-dua momen bon c-cl membatalkan satu sama lain dan molekul mempunyai sifar sifar bersih. Akibatnya, tidak ada daya dipole-dipole intermolecular, yang mengurangkan titik mendidih.
Simetri molekul adalah kunci dalam penentuan titik lebur, kerana pembungkusan bahan pepejal yang lebih baik. Contohnya adalah asid oleik (isomer cis) dan asid elaidik (trans isomer). Titik lebur isomer cis ialah 13.4 ° C, isomer trans cair pada suhu 43 ° C. Sebabnya adalah bahawa isomer trans lebih tegak, pek lebih baik, dan oleh itu - mempunyai titik lebur yang lebih tinggi.
Isomer trans mempunyai kepadatan yang lebih rendah daripada rakan cis mereka. Dalam sistem aciklik, isomer trans lebih stabil daripada isomer cis. Secara umum, isomer cis mempunyai kelarutan yang lebih tinggi dalam pelarut lengai.
Perbezaan antara cis dan trans
-
Definisi cis dan trans
Cis: Awalan "cis" berasal dari bahasa Latin. Itu bermaksud "di sisi yang sama". Di dalam isomer cis, kumpulan substituen diletakkan di satu sisi satah ikatan berganda atau kitaran bukan aromatik.
Trans: Awalan "trans" berasal dari bahasa Latin. Itu bermaksud "pada pihak lawan". Di dalam isomer trans, kumpulan substituen diletakkan di sisi yang berlainan dari satah ikatan berganda atau kitaran bukan aromatik.
-
Titik kutub dan mendidih cis dan trans
Cis: Polariti menyebabkan peningkatan daya intermolecular, yang mengakibatkan peningkatan titik mendidih. Isomer cis, yang lebih kutub daripada isomer trans, mempunyai titik mendidih yang lebih tinggi.
Trans: Isomer trans kurang kutub dan mempunyai titik mendidih yang lebih rendah daripada isomer cis. Perbezaannya lebih penting dalam bahan dengan ikatan kutub.
-
Simetri dan titik lebur cis dan trans
Cis: Isomer cis kurang simetri dan mempunyai titik lebur yang lebih rendah, berbanding dengan isomer trans.
Trans: Isomer trans mempunyai simetri yang lebih tinggi dan titik lebur yang lebih tinggi, berbanding dengan isomer cis.
-
Kestabilan dan kelarutan cis dan trans
Cis: Dalam sistem aciklik, isomer cis lebih tidak stabil daripada isomer trans. Mereka mempunyai keterlarutan yang lebih tinggi dalam pelarut lengai.
Trans: Dalam sistem aciklik, isomer trans lebih stabil daripada isomer cis. Mereka mempunyai kelarutan yang lebih rendah dalam pelarut lengai.
Ringkasan CIS vs. Trans:
- Isomerisme cis-trans terdiri daripada kemungkinan meletakkan kumpulan substituen pada satu atau di sisi yang berlainan satah ikatan berganda atau kitaran bukan aromatik.
- Kewujudan isomer cis dan trans yang berasingan hanya mungkin disebabkan oleh penghalang tenaga tinggi putaran di sekitar ikatan berganda. Mereka ditemui di kalangan sebatian organik dan bukan organik.
- Awalan "cis" dan trans berasal dari bahasa Latin. CIS bermaksud "di sisi yang sama", trans bermaksud "pada sisi lawan".
- Di dalam isomer cis, kumpulan substituen diletakkan di satu sisi, manakala di dalam isomer trans, kumpulan substituen diletakkan di sisi yang berlainan dari satah ikatan berganda atau kitaran bukan aromatik.
- Polariti menyebabkan peningkatan daya intermolecular, yang mengakibatkan peningkatan titik mendidih. Isomer cis lebih kutub daripada isomer trans dan mempunyai titik mendidih yang lebih tinggi. Perbezaannya lebih penting dalam bahan dengan ikatan kutub.
- Isomer cis kurang simetri dan mempunyai titik lebur yang lebih rendah, berbanding dengan isomer trans.
- Dalam sistem aciklik, isomer cis lebih tidak stabil daripada isomer trans. Mereka mempunyai keterlarutan yang lebih tinggi dalam pelarut lengai.