Perbezaan antara koloid dan penggantungan
- 2251
- 596
- Dr. Anthony Turcotte
Sistem penyebaran terdiri daripada dua atau lebih sebatian kimia atau bahan mudah, yang dipanggil komponen sistem, diedarkan antara satu sama lain. Mereka membentuk:
- Fasa tersebar - bahan tersebar;
- Medium berterusan - bahan di mana fasa tersebar diedarkan.
Bergantung pada saiz zarah fasa bersurai ada:
- Sistem penyebaran heterogen (kasar) - zarah lebih besar daripada 100 nm:
- Penggantungan - komponen cecair dan pepejal;
- Emulsi - dua komponen cecair;
- Aerosol - medium penyebaran adalah gas.
- Colloids - Saiz zarah adalah antara 1 dan 100 nm;
- Penyelesaian sebenar - saiz zarah kurang dari 1 nm.

Apa itu Colloid?
Penyelesaian air banyak bahan (gula, dll.), mudah melalui halangan tumbuhan atau haiwan semipermeable, sementara yang lain seperti gelatin tidak melalui mereka. Bahan pertama dipanggil kristal, dan yang kedua dipanggil koloid.
Bergantung pada bagaimana zarah fasa tersebar merujuk kepada medium, sistem koloid adalah:
- Lyophilic - Menyerap Sebilangan besar molekul dari medium penyebaran (gelatin, sabun, Fe (OH)3, Al (oh)3);
- Lyophobic - Jangan mengikat atau mengikat dengan sebilangan kecil molekul dari medium penyebaran (garam logam tertentu, sulfida logam larut yang kurang larut, dll.).
Bergantung pada struktur zarah koloid, sistem koloid dibahagikan kepada:
- Berkaitan (micellar) - zarah adalah kumpulan atom, ion atau molekul (e.g. natrium klorida dalam benzena);
- Molekul - zarah adalah molekul sebatian yang mempunyai jisim molekul yang tinggi (e.g. kanji).
Bergantung pada sifat medium, koloid adalah:
- Hydrosols - Pelarut adalah air;
- Benzenosols - Pelarut adalah benzena;
- Etherosols - pelarut adalah ether dll.
Sifat optik koloid ditunjukkan sebagai pewarna, opalescence, dan kesan tindal. Mereka disebabkan oleh perbezaan penyerapan dan penyebaran cahaya dari zarah koloid.
Zarah koloid lebih besar dan lebih berat daripada ion dan kebanyakan molekul, jadi penyebaran dan tekanan osmotiknya rendah.
Harta kinetik ciri koloid adalah pergerakan Brownian. Sistem koloid kurang stabil daripada penyelesaian biasa. Di bawah arus elektrik yang berterusan, semua zarah koloid bergerak ke elektrod yang bertentangan yang bertentangan. Fenomena ini dipanggil elektroforesis.
Solid koloid molekul diperolehi dengan penyelesaian sebenar. Apabila dihubungi fasa bersurai larut secara spontan dalam medium yang tersebar. SOLs koloid yang berkaitan diperolehi dengan pelbagai kaedah penyebaran dan pemeluwapan.
- Kaedah Penyebaran - Penyebaran bahan kepada saiz zarah koloid dengan kehadiran medium penyebaran;
- Kaedah pemeluwapan - pemeluwapan (pengelompokan) molekul individu, atom atau ion ke dalam zarah saiz koloid.
Apa itu penggantungan?
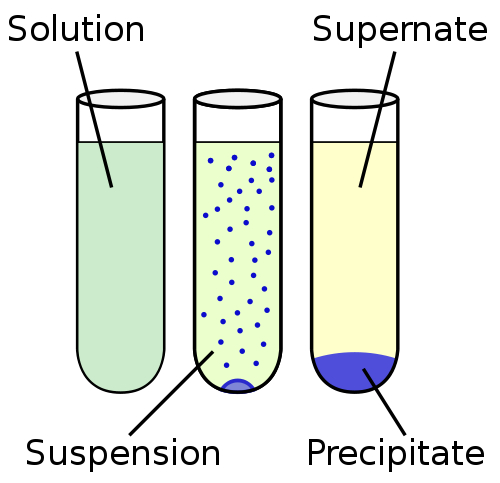
Penggantungan adalah cecair heterogen, yang mengandungi zarah pepejal yang tidak larut yang cukup besar untuk diselesaikan tetapi untuk beberapa waktu hadir sepanjang jumlah matriks cecair. Zarah lebih besar daripada 100 nm.
Klasifikasi penggantungan berdasarkan fasa tersebar dan medium penyebaran.
Penggantungan lebih dekat dengan ketidaksuburan dalam kontinum kelarutan. Di hujung kontinum kelarutan adalah penyelesaian, di mana zarah -zarahnya benar -benar bercampur dan tidak ada fasa pepejal yang diperhatikan. Kekuatan kelarutan umumnya diatur mengikut urutan: ketidaksuburan, pemendapan, penggantungan, koloid dan penyelesaian.
Fasa pepejal penggantungan disebarkan dalam fasa cecair dengan proses pengadukan mekanikal dengan menggunakan ejen aktif atau lemah yang digunakan sebagai ejen penggantungan. Tidak seperti koloid, penggantungan menetap dari masa ke masa. Contoh penggantungan yang cepat adalah pasir dan air.
Harta ciri penggantungan adalah ketidakmampuan optik mereka, yang dinyatakan oleh kekeruhan. Kekeruhan adalah tanda luaran yang penting bagi penggantungan dan ditentukan oleh kehadiran zarah -zarah yang tidak larut yang tidak dapat ditembusi. Tahap kekeruhan penggantungan berbeza. Ia ditentukan oleh kepekatan fasa yang digantung dan tahap penyebarannya (saiz zarah).
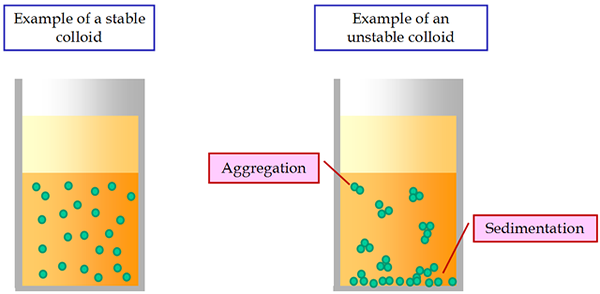
Salah satu ciri yang paling penting dalam penggantungan adalah ketidakstabilan pemendapan mereka. Ia dinyatakan dalam penyelesaian yang tidak dapat dielakkan dari zarah yang digantung di bawah pengaruh graviti. Zarah dapat menyelesaikannya sendiri, tanpa melekat bersama. Dalam kes ini terdapat kestabilan agregat penggantungan.
Sekiranya zarah penyelesaian melekat bersama di bawah pengaruh daya molekul perpaduan dan bentuk agregat, maka terdapat ketidakstabilan agregatif penggantungan. Oleh itu, penggantungan sedimentasi yang tidak stabil boleh menjadi agregat stabil atau tidak stabil.
Kadang -kadang dalam penggantungan yang menggosok, serpihan besar terbentuk yang kurang dibasuh oleh medium penyebaran dan terapung ke permukaan. Fenomena ini dipanggil pemberbukuan.
Ketidakstabilan pemendapan penggantungan dalam amalan membawa kepada gangguan secara beransur -ansur komposisi seragam sebelum pemendapan lengkap fasa tidak larut.
Terdapat juga penggantungan, mempunyai keupayaan untuk kekal dalam keadaan yang digantung untuk masa yang lama. Mereka dipanggil penggantungan stabil.
Penggantungan diperolehi oleh pelbagai kaedah penyebaran dan pemeluwapan.
Perbezaan antara koloid dan penggantungan
-
Definisi
Colloid: Sistem penyebaran dengan komponen cecair dan pepejal, dengan saiz zarah antara 1 dan 100 nm dipanggil koloid.
Penggantungan: Sistem penyebaran dengan komponen cecair dan pepejal, dengan saiz zarah melebihi 100 nm dipanggil penggantungan.
-
Saiz Zarah
Colloid: Saiz zarah ialah 1-100 nm.
Penggantungan: Saiz zarah melebihi 100 nm.
-
Penglihatan zarah
Colloid: Zarah -zarah di koloid tidak dapat dilihat dengan mata kasar.
Penggantungan: Zarah dalam penggantungan dapat dilihat dengan mata kasar.
-
Pemendapan
Colloid: Koloid tidak menjalani pemendapan.
Penggantungan: Penggantungan menjalani pemendapan.
-
Homogeniti
Colloid: Koloid agak homogen.
Penggantungan: Penggantungannya heterogen.
-
Kebolehtelapan melalui kertas penapis
Colloid: Zarah koloid boleh melalui kertas penapis.
Penggantungan: Zarah penggantungan tidak dapat melalui kertas penapis.
-
Contoh
Colloid: Gelatin di dalam air, kanji di dalam air, natrium klorida dalam benzena, dll.
Penggantungan: Pasir di dalam air, kapur serbuk di dalam air, merkuri dalam minyak, dll.
Carta perbandingan koloid dan penggantungan
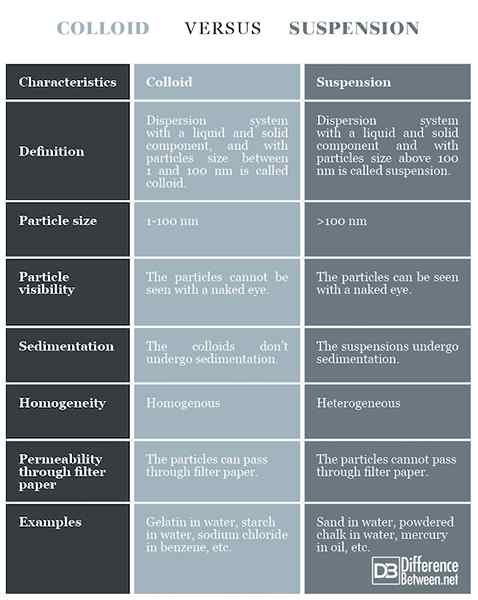
Ringkasan koloid dan penggantungan
- Sistem penyebaran terdiri daripada dua atau lebih sebatian kimia atau bahan mudah, yang dipanggil komponen sistem, diedarkan antara satu sama lain. Mereka membentuk fasa tersebar dan medium yang berterusan.
- Sistem penyebaran dengan komponen cecair dan pepejal, dengan saiz zarah antara 1 dan 100 nm dipanggil koloid.
- Sistem penyebaran dengan komponen cecair dan pepejal, dengan saiz zarah melebihi 100 nm dipanggil penggantungan.
- Zarah -zarah di koloid tidak dapat dilihat dengan mata kasar, sementara zarah -zarah dalam penggantungan dapat dilihat dengan mata kasar.
- Koloid tidak menjalani pemendapan, sementara penggantungan menjalani pemendapan.
- Koloid agak homogen, sementara penggantungannya heterogen.
- Zarah koloid boleh melalui kertas penapis, sementara zarah penggantungan tidak dapat.
- Contoh koloid adalah gelatin di dalam air, kanji di dalam air, natrium klorida dalam benzena, dll. Contoh penggantungan adalah pasir di dalam air, kapur serbuk di dalam air, merkuri dalam minyak, dll.

