Perbezaan antara jisim molar dan jisim molekul
- 4811
- 998
- David Collier
Ahli kimia kerap mengukur bahan dengan menggunakan jisim molar dan jisim molekul. Contohnya ialah menentukan bilangan molekul dalam silinder. Kimia mengkaji interaksi atom dan molekul pada skala atom.

Berapakah jisim molekul?
Pertama, molekul merujuk kepada komposisi atom yang serupa atau berbeza yang diatur dalam nisbah. Molekul boleh membentuk sebatian kimia tertakluk kepada sifat fizikal dan kimia setiap molekul.
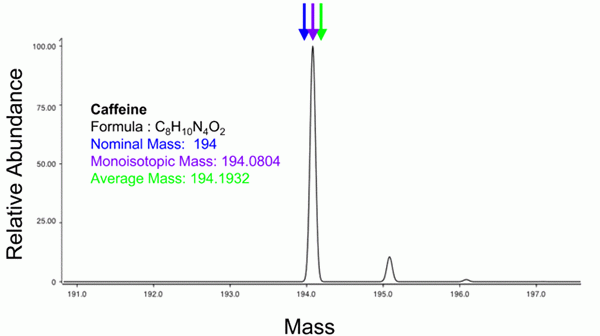
Ringkasnya, jisim molekul merujuk kepada jumlah jisim bahan. Ia merangkumi purata jisim atom individu dalam molekul bahan tertentu.
Untuk menentukan jisim molekul sebatian x, anda perlu menambah massa atom semua elemen dalam komposisi termasuk pendaraban mereka mengikut subskrip dalam formula.
Kami akan menggambarkan dengan contoh di bawah. Jisim atom ini diambil secara langsung dari jadual unsur berkala. Mereka diukur dalam unit jisim atom (amu) dan begitu juga jisim molekul.
Contoh 1:
Tentukan jisim molekul H2O dan CH3CH2OH.
Jawapan:
Anda perlu menilai komposisi formula molekul yang diberikan dan memperoleh massa atom mereka dari jadual berkala. Ambil kira subskrip.
Sebagai contoh, H2O menunjukkan bahawa terdapat dua atom hidrogen dan satu atom oksigen. Jisim atom hidrogen adalah, dari jadual berkala, 1.0079 amu dan oksigen adalah 15.9994. Jisim molekul sebatian adalah 2 (1.0079) + 15.9994 = 18.0152 Amu.
Dan untuk menentukan jisim molekul etanol, formula lain yang diberikan dalam soalan, kita mengikuti langkah yang sama. Terdapat 2 atom karbon, 6 atom hidrogen dan 1 atom oksigen. Jisim atom atom karbon adalah 12.011 amu. Yang mengatakan, jisim molekul CH3CH2OH adalah 2 (12.011) + 6 (1.0079) + 1 (15.9994) = 46.069 amu. Untuk latihan anda, hitung formula molekul etana (C2H4) dan CO2.
Apa itu jisim molar?
Sekarang mengenai konsep massa molar, ia ditakrifkan sebagai jisim dalam kilogram atau gram mole bahan. Biasanya, unit untuk jisim molar adalah gram/mol. Tahi lalat elemen oksigen mempunyai jisim 15.9994 gram. Oleh itu jisim molar akan menjadi 15.9994 g/mol. Untuk sebatian karbon dioksida, contohnya, jisim molar ditakrifkan sebagai jisim 1 mol molekul di kawasan itu. Nombor Avogadro, 6.022 x 1023 sering digunakan untuk mengaitkan bilangan atom, molekul dan unit lain bahawa jisim molar sama dengan. Sebagai contoh, jisim molar H2O akan sama dengan jisim dalam gram per mole 6.022 x 1023 molekul air. Jika ini terdengar terlalu teknikal, kami akan menggambarkan dengan contoh di bawah:
Contoh 2:
Tentukan jisim molar etanol.
Jawapan:
Dalam contoh pertama, kami menentukan jisim molekul etanol (C2H5OH). Jangan dikelirukan oleh formula yang berbeza seperti yang dinyatakan di atas. Kami baru sahaja bermain -main dengan pengaturan struktur formula etanol walaupun nisbah atom tetap sama.
Ethanol mengandungi 6.022 x 1023molecules, dan jisim molar sama dengan jisim etanol yang mengandungi molekul ini. Kami menjumpai jisim molekul etanol menjadi 46.069 Unit Massa Atom Dalam contoh terdahulu kami. Prosedur yang sama diikuti dalam mengira jisim molar.
Satu mol etanol mempunyai atom karbon 2 mol, 6 mole atom hidrogen dan satu mol atom oksigen. Mengambil jisim atom dari jadual tempoh, kita mendapati bahawa jisim molar adalah 2 (12.011g) + 6 (1.0079g) + 15.9994G yang sama dengan 46.069 g/mo. Perhatikan nilai yang sama tetapi unit yang berbeza.
NB: Jisim molar dari mana -mana bahan kimia merujuk kepada jisim atom atau jisim molekulnya dalam gram setiap tahi lalat. Nilai adalah sama tetapi berbeza unit.
Latihan 2:
Kirakan jisim molar kalsium fosfat (CA3 (PO4) 2). Jawapannya hendaklah 310.177 g/mol.
Berkenaan dengan karbon, jisim molar karbon yang semulajadi dengan berbeza dari yang diperoleh dari jadual tempoh yang dimiliki oleh isotop karbon-12. Secara semulajadi, karbon mengandungi karbon-12, karbon-13 dan karbon-14. Tetapi tahi lalat karbon masih mengandungi 6.022 x 1023 tetapi dengan nisbah yang berbeza dari isotop ini.
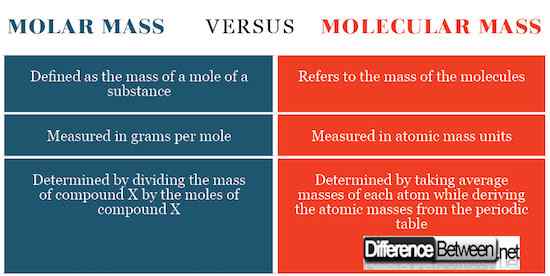
Perbezaan antara jisim molar dan jisim molekul
Pengiraan jisim molar dan jisim molekul
Jisim molar ditentukan dengan membahagikan jumlah jisim bahan yang merupakan jisim purata setiap atom dengan jumlah moles. Angka yang dihasilkan akan menjadi gram per mol atau kilogram setiap tahi lalat. Jisim molekul ditentukan dengan mengira jisim bahan yang berkaitan dengan 1/12 isotop karbon-12.
Definisi jisim molar dan jisim molekul
Jisim molekul merujuk kepada jisim molekul manakala jisim molar merujuk kepada jisim tahi lalat bahan.
Unit Si untuk jisim molar dan jisim molekul
Jisim molar dinyatakan sebagai gram per mole manakala jisim molekul dinyatakan sebagai unit jisim atom. Ekspresi unit Si ini kembali kepada bagaimana konsep -konsep ini ditakrifkan sebagai disebutkan di atas.
Ringkasan jisim molar vs. Jisim molekul
- Jisim molar dan jisim molekul adalah konsep penting dalam kimia
- Jisim molar dinyatakan dalam gram per mol atau kilogram per mole manakala jisim molekul dinyatakan dalam unit jisim atom. Jisim molar pada dasarnya tidak unit.
- Kami mengira jisim molar dengan membahagikan jisim bahan dengan jumlah dan mengira jisim molekul dengan mengambil jisim purata unit bahan
- Mereka mempunyai nilai yang sama tetapi unit SI yang berbeza.

